对细胞内相关蛋白酶的原位成像检测具有非常重要的生物医学意义。过去几十年中,小分子荧光探针已经广泛用于细胞内各种酶活性的检测与成像研究。然而,已有的荧光探针大多是基于水溶性荧光染料,与酶作用后产生的荧光信号分子会快速扩散远离酶的反应位点,很难捕获细胞内相关酶的原位信息。日前,由我校化学生物传感与计量学国家重点实验室、化学化工学院和生物学院共同建设的"分子科学与生物医学实验室(MBL实验室)"张晓兵教授研究团队,开发出新型适用于商业激光共聚焦显微镜的固态发光荧光染料,并进一步构建了酶荧光成像探针,实现了活细胞内碱性磷酸酶活性的原位成像检测。
相关研究成果以"In Situ Localization of Enzyme activity in Live Cells by a Molecular Probe Releasing a Precipitating Fluorochrome"为题发表于国际顶尖化学期刊《德国应用化学》(Angew. Chem. Int. Ed. 影响因子11.994)。
三氧化二砷(As2O3, ATO, 俗称砒霜),一种经典的剧毒中药,现已成为全球治疗急性早幼粒细胞白血病(APL)白血病的标准药物之一,其治疗完全缓解率高达83-95%。鉴于砒霜治疗APL的有效性,广大科学工作者致力于探索与拓展ATO用于其它恶性白血病(如慢性髓性白血病CML)和实体瘤的治疗。然而,ATO在非APL癌细胞中富集能力弱,高剂量的治疗模式会引起神经损伤和肝功能衰竭等严重毒副作用,因此大大限制了ATO在其它癌症中的临床应用。
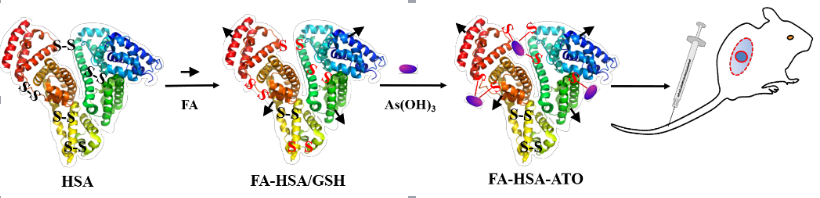
针对这一难题,我校化学生物传感与计量学国家重点实验室、化学化工学院和生物学院共同建设的"分子科学与生物医学实验室(MBL)"基于ATO易与游离巯基形成AsIII-S键的化学性质,利用还原剂将叶酸-人血清白蛋白(FA-HSA)的双硫键打开,然后与ATO孵育,发展了叶酸受体靶向的FA-HSA-ATO纳米药物。相关成果发表在Angewandte Chemie International Edition, 2017, DOI: 10.1002/anie.201701366.
该纳米药物具有以下几个优点:(1)制备简单,且具有良好的生物兼容性;(2)弱酸性和胞内谷胱甘肽响应的ATO释放,减少了ATO的非特异性分布;(3)有效地诱导CML肿瘤细胞叶酸受体表达,增强纳米药物在CML肿瘤细胞中的富集。
基于FA-HSA-ATO纳米药物的上述优点,该纳米药物能显著抑制K562移植瘤的生长,延长带瘤裸鼠中位生存期,同时有效减少ATO在治疗中的毒副作用。该工作为拓展ATO在慢性髓性白血病和其他肿瘤的临床应用提供了新的方法和思路。目前该课题组正在进行进一步的研究,争取开发相关的临床应用的治疗方案。
文章链接:http://onlinelibrary.wiley.com/doi/10.1002/anie.201701366/full
文章作者:Yongbo Peng, Zilong Zhao, Teng Liu, Xiong Li, Xiaoxiao Hu, Xiaoping Wei, Xiaobing Zhang, and Prof. Weihong Tan